Xét nghiệm đột biến gene trong điều trị ung thư tại Việt Nam đang được quy định như nào?
Cá thể hóa điều trị trong ung thư đem lại cơ hội điều trị thành công và sống còn cho bệnh nhân ta·, nhưng trong hệ thống y tế đang vận hành, vẫn có những mảnh ghép xám nên được bàn luận và đưa ra ánh sáng trong thời điểm hiện tại.

Theo Globocan, năm 2022 Việt Nam có 180.480 ca ung thư mắc mới, 120.184 ca tử vong liên quan đến ung thư. Trong đó bệnh lý ung thư mắc nhiều nhất lần lượt: Gan, Phổi, Dạ dày, Đại trực tràng.
Những năm gần đây, liệu pháp điều trị đích cá thể hóa hay còn gọi điều trị thuốc đích trong ung thư đang được áp dụng rộng rãi trong thực hành lâm sàng để tăng cơ hội sống khỏe mạnh, giảm tiến triển khối u, giảm tác dụng phụ... đem lại vượt trội hơn hẳn trong một số trường hợp. Để xác định bệnh nhân có thể dùng thuốc đích hay không, bắt buộc bệnh nhân phải được xét nghiệm sinh học phân tử chẩn đoán gene mang đột biến.
Ngành sinh học phân tử, chẩn đoán gene tại Việt Nam tuy đã có nhiều bước tiến, song vẫn còn một số bất cập, đặc biệt là các xét nghiệm chuyên sâu kỹ thuật cao như NGS (Giải trình tự gene thế hệ mới), bệnh nhân và người nhà nếu không có chuyên môn, khó có thể tìm hiểu thông tin cơ bản về các xét nghiệm có giá đến hàng triệu thậm chí chục triệu đồng này. Đặc biệt quy định của pháp luật Việt Nam hiện nay với các xét nghiệm này đang như nào?
Bài viết này được tổng hợp các thông tin chuyên môn với mục tiêu trình bày dễ hiểu và logic cho mọi người, kể cả người không có chuyên môn về xét nghiệm đặc biệt là các xét nghiệm kỹ thuật cao. Thông qua đó, bạn đọc được hiểu rõ bản chất cũng như nắm rõ quy định pháp luật Việt Nam về xét nghiệm để tự phản biện lại những quảng cáo mỹ miều chỉ tập trung vào công nghệ cao, xuất xứ Hoa Kỳ… mà ít đề cập đến những yếu tố cốt lõi.
1. Pháp luật quy định
Trang thiết bị y tế được phép lưu hành và làm xét nghiệm thu phí trên lãnh thổ Việt Nam cần phải tuân thủ Nghị định số 98/2021/NĐ-CP và Thông tư: 05/2022/TT-BYT.
1.1 Nghị định số 98/2021/NĐ-CP của Chính phủ
Quy định về việc đăng kí và lưu hành đối với trang thiết bị y tế có định nghĩa trong Điều 2:
Định nghĩa: Trang thiết bị y tế là các loại thiết bị, vật tư cấy ghép, dụng cụ, vật liệu, thuốc thử và chất hiệu chuẩn in vitro, phần mềm (software)...
Như vậy, không chỉ thiết bị máy móc thực hiện xét nghiệm cần phải đăng ký lưu hành mà hóa chất, thuốc thử, chất chuẩn, và cả phần mềm phân tích kết quả xét nghiệm cũng cần đăng kí lưu hành tại Việt Nam.
Ngoài ra, Điều 4. Chương II- Nghị định số 98/2021/NĐ-CP
Loại trang thiết bị y tế
Trang thiết bị y tế được phân làm 4 loại dựa trên mức độ rủi ro tiềm ẩn liên quan đến thiết kế kỹ thuật và sản xuất các trang thiết bị y tế đó: 1. Trang thiết bị y tế thuộc loại A là trang thiết bị y tế có mức độ rủi ro thấp. 2. Trang thiết bị y tế thuộc loại B là trang thiết bị y tế có mức độ rủi ro trung bình thấp. 3. Trang thiết bị y tế thuộc loại C là trang thiết bị y tế có mức độ rủi ro trung bình cao. 4. Trang thiết bị y tế thuộc loại D là trang thiết bị y tế có mức độ rủi ro cao.
1.2 Hướng dẫn phân loại
Thông tư: 05/2022/TT-BYT, Phần III, Quy tắc 3 có quy định:
Trang thiết bị y tế chẩn đoán in vitro sử dụng cho một trong các mục đích sau thì được xếp vào loại C: 6. Sàng lọc lựa chọn bệnh nhân để áp dụng biện pháp quản lý và liệu pháp điều trị phù hợp hoặc để xác định giai đoạn của bệnh hoặc chẩn đoán ung thư (ví dụ y học cá thể hóa). 7. Xét nghiệm gen di truyền ở người (ví dụ như bệnh Huntington, xơ nang).
Như vậy, các quy định rất chặt chẽ với xét nghiệm liên quan đến điều trị ung thư, bắt buộc phải đăng kí trang thiết bị y tế loại C.
Thực tế thì vẫn có những đơn vị lách luật, đăng kí thiết bị y tế loại B với xét nghiệm liên quan đến ung thư.
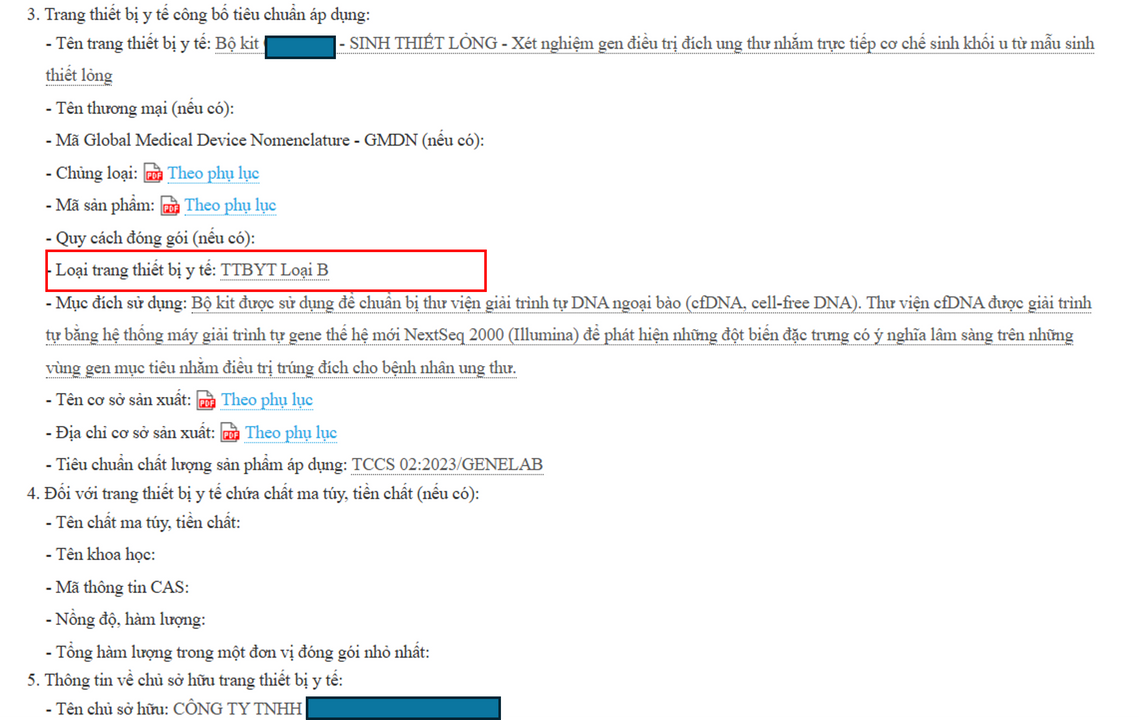
Hồ sơ đăng ký này hiện đã bị thu hồi. Một số phần đã được che tên để tránh đánh giá bài viết mang tính công kích.
Tại sao các công ty lại lách luật như vậy?
Câu trả lời là:
1.3 LUẬT KHÁM BỆNH, CHỮA BỆNH 2023
Khoản 2 Điều 94 trong luật khám chữa bệnh quy định:
Các trường hợp thử nghiệm lâm sàng trong khám bệnh, chữa bệnh: 1. Kỹ thuật mới, phương pháp mới trong khám bệnh, chữa bệnh. 2. Thiết bị y tế trước khi đăng ký lưu hành tại Việt Nam có mức độ rủi ro trung bình cao hoặc mức độ rủi ro cao theo quy định của Chính phủ.
Như vậy những thiết bị y tế loại C vốn có mức độ rủi ro trung bình cao cần phải làm thử nghiệm lâm sàng, còn loại B thì không bắt buộc. Để tối ưu chi phí, tiết kiệm thời gian hoặc lý do nào đó liên quan đến chất lượng,... một số công ty đã bỏ qua thử nghiệm lâm sàng và đưa sản phẩm rủi ro cao đến với người bệnh.
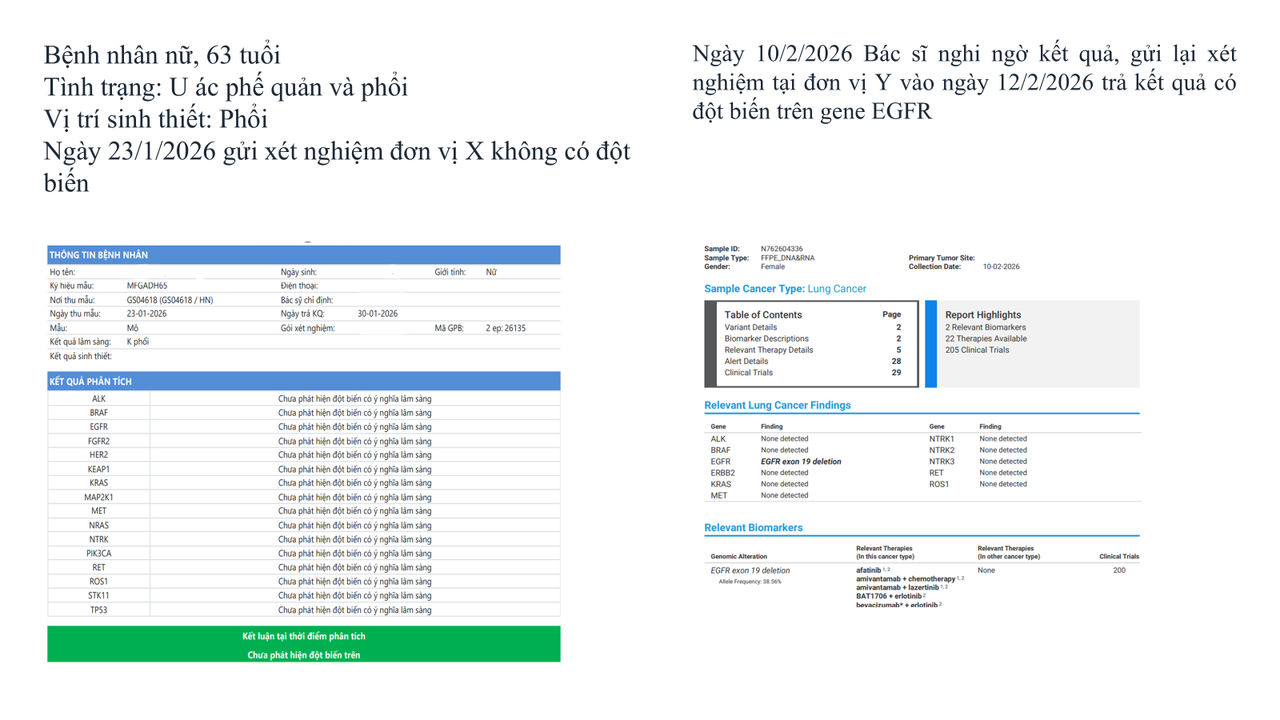
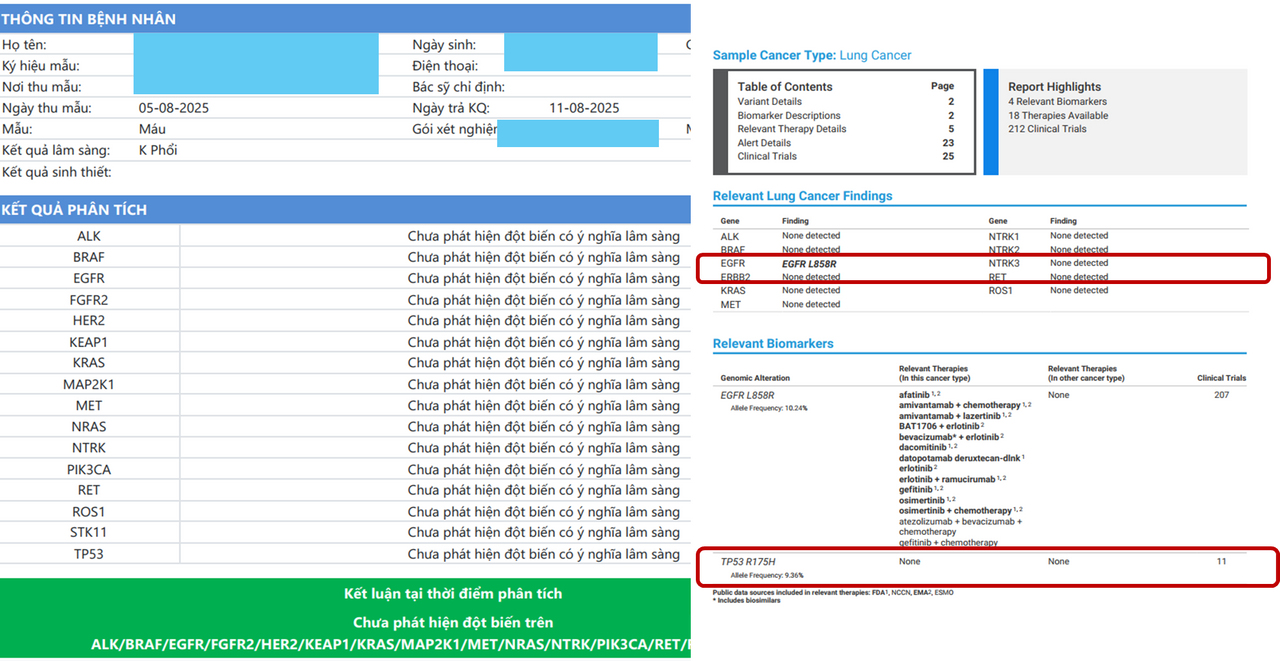
Và những rủi ro đó thực sự đã xảy ra trên thực tế điều trị, với những xét nghiệm âm tính giả đã bỏ lỡ cơ hội điều trị tốt cho bệnh nhân. Dưới đây là một case lâm sàng khi xét nghiệm ở đơn vị thứ nhất kết luận không có đột biến. Nhưng khi được thực hiện lại với đơn vị thứ 2 (tuân thủ đúng quy định đăng kí lưu hành trang thiết bị) thì đã xuất hiện đột biến EGFR exon 19, một đột biến phổ biến ở bệnh nhân ung thư phổi không tế bào nhỏ (NSCLC).
Nếu không có hướng dẫn, truyền thông sớm về chất lượng xét nghiệm di truyền, liệu bao nhiêu người nữa sẽ bị âm tính giả, bác sĩ bỏ sót hướng điều trị tối ưu, và chính bệnh nhân là người thiệt thòi nhất khi bỏ lỡ cơ hội điều trị, bỏ lỡ cuộc sống bên gia đình đang chờ đợi?
2. IVD và RUO
Trong phần một, nếu bạn để ý trong nghị định có nhắc đến in vitro nhiều lần, chỉ những trang thiết bị được chứng nhận in vitro hay còn gọi IVD mới được phép lưu hành, kinh doanh tại lãnh thổ Việt Nam. Đây là một khái niệm rất quan trọng trong mảng xét nghiệm mà giới lâm sàng hoặc người ngoại đạo chưa quen thuộc.
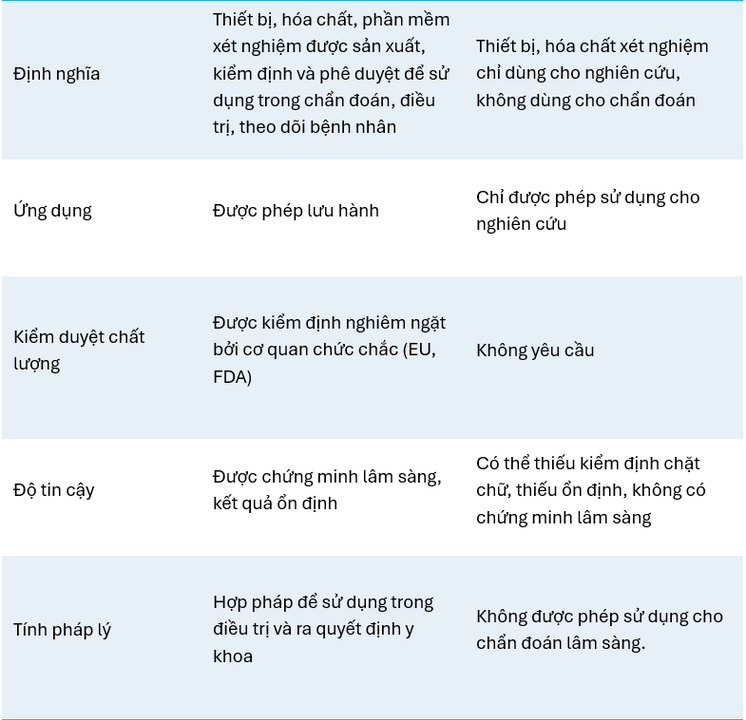
Trang thiết bị dùng xét nghiệm ở Việt Nam được chia làm 3 loại tiêu chuẩn chính: IVD (dùng để xét nghiệm phục vụ mục tiêu lâm sàng và có thể thu phí), RUO (Research Use Only - Chỉ sử dụng trong nghiên cứu), ngoài ra còn tiêu chuẩn LUO (Laboratory Use Only - Chỉ dùng cho phòng thí nghiệm) nhưng ít gặp. Bảng dưới đây so sánh điểm khác nhau giữa tiêu chuẩn IVD và RUO.
Với xét nghiệm đạt tiêu chuẩn IVD đặc biệt CE-IVD (tiêu chuẩn IVD của Liên minh Châu Âu) hoặc IVD do FDA cấp phép là cơ sở đảm bảo độ tin cậy của xét nghiệm, giúp quyết định lâm sàng chính xác, kết quả được minh chứng trên các nghiên cứu thử nghiệm nghiêm ngặt.
“ CHÍNH XÁC – TIN CẬY – AN TOÀN”
3. Những câu hỏi cần đặt ra
Với tinh thần, bệnh nhân/khách hàng có quyền được biết chất các xét nghiệm mà mình được chỉ định có đúng quy định không.
Tại phần này mình sẽ hệ thống một số câu hỏi cơ bản để bệnh nhân, hoặc người thân có thể trao đổi với cán bộ y tế về xét nghiệm di truyền trong sàng lọc điều trị ung thư hoặc chẩn đoán trước sinh mà sắp phải tri trả.
1. Xét nghiệm này, đã được đăng ký toàn bộ quy trình từ: thiết bị, hóa chất, phần mềm, thuốc thử chưa?
2. Nếu đã đăng ký toàn bộ, thì giấy phép lưu hành là trang thiết bị y tế loại gì? A,B,C,D?
3. Bộ Kit đã đạt chuẩn IVD chưa, nếu có thì IVD của vùng lãnh thổ nào nào? Hoa Kỳ, EU, Úc hay Canada,...
4. Bộ kit thuốc thử đã được đăng ký loại C vậy thử nghiệm lâm sàng đã công bố đâu, và nếu là xét nghiệm NGS thì có so sánh đối chiếu với kỹ thuật nào?
Theo cá nhân mình, với 4 câu hỏi này, dù bạn không phải là người có chuyên môn nhưng phần nào biết về chất lượng xét nghiệm mà mình sắp phải chi trả đã đạt chuẩn chưa.
Kết bài: những thông tin này do mình và đồng nghiệp tìm hiểu và tổng hợp lại thành bài viết. Nếu có thiếu sót, rất mong nhận được góp ý từ bạn đọc để hoàn thiện và đóng góp phần nhỏ cho những bệnh nhân ung thư đang phải vượt qua vô vàn khó khăn.
Xin được cảm ơn Dược sĩ Đ.H.C, Thạc sĩ N.H.A đã cùng tìm hiểu và thu thập các thông tin trong bài.

Khoa học - Công nghệ
/khoa-hoc-cong-nghe
Bài viết nổi bật khác
- Hot nhất
- Mới nhất